Открытие нейробиологов показало, как возникает эмпатия

Исследовательская группа под руководством доктора Кеум Сехуна из Центра познания и социальности (CCS) при Институте фундаментальных наук (IBS) в Южной Корее показала, как мозг обрабатывает чужой дистресс. Работа опубликована в журнале Nature Communications.
Используя миниатюрную эндоскопическую визуализацию кальция, исследователи выявили специфические нейронные ансамбли в передней поясной коре (ППК), которые кодируют эмпатическое «замирание» — поведенческую реакцию, при которой наблюдатель испытывает страх, наблюдая дистресс у других людей. (Дистресс — состояние страдания, при котором человек не может полностью адаптироваться к стрессовым факторам и вызванному ими стрессу и демонстрирует дезадаптивное поведение.)
Центр сопереживания — передняя поясная кора
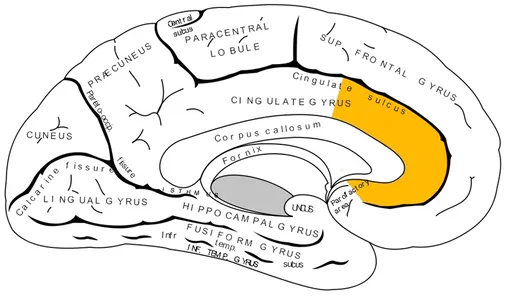
Чтобы изучить этот феномен, команда провела серию экспериментов по визуализации мозга мышей в режиме реального времени. Ученые отслеживали отдельные нейроны мыши, когда она наблюдала за другой мышью, испытывающей легкий удар).
Результаты показали, что определенные нейроны ППК активировались как при непосредственном переживании боли наблюдателем, так и при наблюдении за болью другой особи. Это подтверждает предположение, что наблюдение за дистрессом вызывает нейронную реакцию, сходную с непосредственным переживанием боли.
Исследование также показало, что активность нейронов ППК во время эмпатического замирания очень похожа на нейронное представление переживаемых, но не сенсорных аспектов непосредственного переживания боли. Так человек реагирует на угрозу, которая не воплотилась, а, возможно, и не воплотиться в действие.
Это говорит о том, что наблюдение за чужой болью вызывает активацию ППК, как если бы наблюдатель сам испытывал боль, что подчеркивает специализированную роль ППК в обработке эмоциональных (а не физических) аспектов боли.
Дальнейший анализ показал, что нейроны ППК, воздействуют на околоводопроводное серое вещество (ОСВ), — область мозга, участвующую в регуляции страха и боли. ППК избирательно передают информацию об эмоциональной боли.
Нейронный путь чужой боли

Исследователи использовали оптогенетику, технику, которая позволяет точно контролировать нейронную активность с помощью света. Когда ученые подавляли цепь ППК-ОСВ, эмпатическое замирание и поведение избегания боли значительно снижались. Это подтверждает, что этот путь трансформирует воспринимаемый дистресс в поведенческие реакции.
В отличие от предыдущих исследований, которые были сосредоточены на животных с предшествующим опытом боли, в этом исследовании использовались наивные мыши-наблюдатели, которые ранее не подвергались воздействию боли, что позволило исследователям изучить чистое эмоциональное «заражение» без влияния прошлого опыта. Этот подход дает новое представление о фундаментальных нейронных механизмах аффективной эмпатии.
Понимание того, как мозг кодирует эмпатию, может иметь важные последствия для исследований в области психического здоровья. Такие состояния, как расстройство аутистического спектра (РАС), антисоциальное расстройство личности, ПТСР и шизофрения, часто связаны с трудностями в обработке социальных и эмоциональных сигналов.
Выявив конкретные мозговые контуры, участвующие в обмене аффектами, ученые могут разработать новые стратегии лечения этих расстройств.
Доктор Кеум Сехун говорит: «Наши результаты указывают на конкретные мозговые контуры, участвующие в эмоциональной обработке боли других, предлагая основу для новых подходов к изучению нейропсихиатрических расстройств, связанных с эмпатией».
